

全新靶点+候选药物!郁金泰教授团队在帕金森病治疗领域取得历史性突破
发布日期:2025-02-24 17:16:55 作者: 来源:
浏览次数:38699
近日,我院副院长郁金泰教授所带领的国家神经疾病医学中心、脑功能与脑疾病全国重点实验室、复旦大学附属华山医院团队在帕金森病治疗领域实现历史性突破,为全球神经退行性疾病治疗开辟新纪元。相关成果引起广泛关注,被《科学》(Science)杂志审稿人评价为“PD领域圣杯性的研究工作”。
据悉,郁金泰教授带领团队在全球范围内首次发现帕金森病的全新治疗靶点FAM171A2,并基于该靶点发现可以延缓病程的候选药物,有望从疾病早期对帕金森病进行诊断和干预。其相关研究成果于北京时间2月21日在线发表于国际学术期刊《科学》(Science)。就在上个月,该团队刚有成果登上《细胞》(Cell)杂志的开年封面。
此项历时五年的临床和基础研究首次发现帕金森病全新治疗靶点FAM171A2,并基于该靶点发现可以延缓病程的候选药物,有望从疾病早期对帕金森病进行诊断和干预,结合现有的对症治疗手段,可实现对帕金森病的“标本兼治”,造福百万帕金森病患者。
值得一提的是,此次发现的蛋白靶点极具创新性,在此之前,学界尚未有关于这一蛋白的任何功能性实验研究。课题组下一步将进一步明确该蛋白在神经系统的生理和病理功能,探究该蛋白是否也可作为其他α-突触核蛋白疾病和其他神经退行性疾病的干预靶点。
“从0到1”:首次破解帕金森病核心机理,发现全新治疗靶点
帕金森病(Parkinson's disease,简称PD)是仅次于阿尔茨海默病的第二常见的神经退行性疾病,严重影响患者日常生活,致残率和死亡率较高。全球帕金森病患病人数预计将从2015年的700万左右增至2040年的1300万,我国帕金森病患者总数约占全球一半。
然而,传统药物和手术治疗都只是针对症状进行治疗,比如补充多巴胺、使用脑起搏器,都不能延缓疾病进展。
“帕金森病的现有手段主要针对‘治标’,我们想在‘治本’方面取得新突破,从而实现‘标本兼治’。”在神经退行性疾病领域深耕近二十年的郁金泰,一直希望攻克这一重大医学难题。
已有研究表明,病理性α-突触核蛋白是帕金森病的关键致病蛋白。α-突触核蛋白的错误折叠和异常聚集,会导致神经元死亡,还会像“种子”一样播散,入侵邻近的正常神经元,诱导更多脑区α-突触核蛋白聚集和神经元死亡。而其中传播环节具体到底怎样进行,又有哪些关键受体,始终未能明晰。
▲
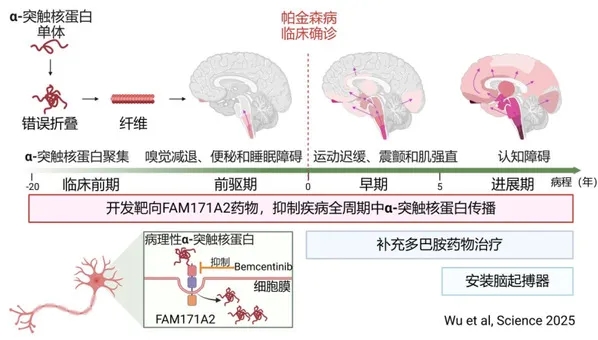
帕金森病病程进展机制及干预手段
通过长达5年的潜心钻研,郁金泰团队明确了病理性α-突触核蛋白在神经元间的传播“导火索”,并发现了阻断其传播过程的候选新药,为帕金森病治疗提供了新思路。
团队最初从大规模人群的全基因组关联分析中,发现FAM171A2是帕金森病风险基因。经过系列研究,团队证实神经元膜受体FAM171A2蛋白是促进病理性α-突触核蛋白传播的关键,在全球首次揭示了FAM171A2蛋白与α-突触核蛋白的结合机制。
基于帕金森病患者临床样本分析,团队发现帕金森病患者大脑中FAM171A2蛋白含量增高,且FAM171A2含量越高的患者,其脑内病理性α-突触核蛋白含量也越高。
通过一系列体内外实验,研究团队发现在神经元细胞膜上,FAM171A2像“智能识别门”一样,可选择性地结合病理性α-突触核蛋白,并携带其进入到神经元中,诱导神经元内单体形式的α-突触核蛋白发生错误折叠,造成神经元死亡和其在神经元间的传播。随后,研究团队通过转基因动物证实,敲除小鼠神经元上FAM171A2,可以有效控制小鼠帕金森样症状的进展。
▲
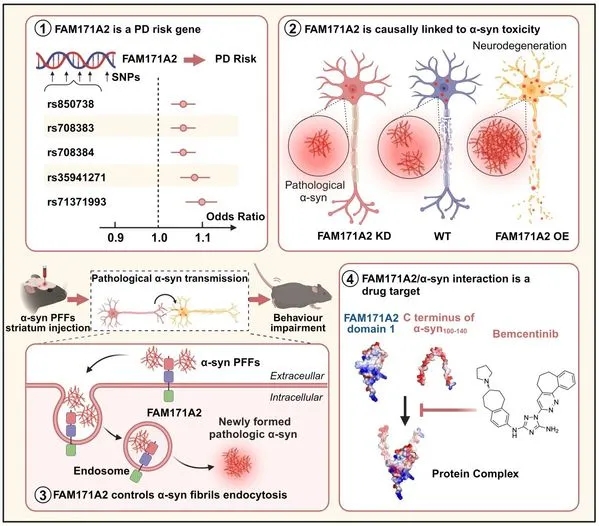
帕金森病风险基因FAM171A2可特异性结合病理性ɑ-突触核蛋白,加速其在神经元间传播。小分子bemcentinib可抑制FAM171A2和病理性ɑ-突触核蛋白结合
帕金森病患者在出现运动症状之前十几年,大脑内就已存在α-突触核蛋白病理。本次研究发现有望在疾病的临床前期、前驱期和临床期通过靶向抑制原创新靶点FAM171A2以阻断病理性α-突触核蛋白传播,延缓帕金森病进展。
AI赋能:突破现有知识体系,精准高效筛选未知靶点和分子药物
对PD核心病理的研究,一直是全球相关领域科学家竞相探索的战略高地。此前也曾有一些国际研究团队对病理性α-syn的传播机制进行研究,提出一些潜在受体,但验证效果并不尽如人意。
“这的确是一项非常艰难的工作,因为神经系统本身非常复杂。”郁金泰认为,复旦团队之所以能够发现FAM171A2这一全新靶点,与采取AI辅助、数据驱动的创新科研范式息息相关。

▲
郁金泰教授
过去,帕金森病研究主要采用“假说驱动”的研究范式——研究者根据现有理论体系,推测某一蛋白可能在病理性α-突触核蛋白传播过程中发挥重要作用,再设计实验进行证实。但人体内的基因蛋白数量极其庞大,采用这一方法意味着忽略了现有理论体系外的诸多可能性。
相比之下,“数据驱动”则是一种不带预设的研究思路。在组学技术和数据分析技术快速发展的背景下,郁金泰团队突破“假说驱动”研究范式,在所有基因中筛选潜在靶点,再进行体内外基础实验加以验证。
“我们就是要分析所有能分析的数据,看看到底哪个蛋白效果更好。” 通过大规模人群全基因组关联分析研究,团队最终在数万个基因中找到了“嫌疑最大”的目标靶点——FAM171A2。
这个“神秘”的神经元细胞膜蛋白此前从未被学界关注,没有任何参考文献。研究一作、复旦大学附属华山医院博士后吴凯敏记得,为了摸索FAM171A2如何参与帕金森病,花了一年左右时间确定实验条件。
“基于传统研究范式,我们是不可能发现它的,只有在数据驱动下进行筛选,才能找到它。”郁金泰认为。


紧接着,团队趁热打铁,继续寻找能够干预靶点、阻断病理性α-syn传播的小分子药物。但由于团队对FAM171A2的结构一无所知,且小分子库中的候选者成千上万,若是按照传统方法解析结构、挨个筛选,无异于是大海捞针,这也是此前相关研究成功率低的关键原因。
这时,AI for Science再次“大显身手”。团队利用人工智能技术对其蛋白结构进行预测,再基于预测结构对小分子化合物进行虚拟筛选。
“根据AI预测出来的蛋白结构,我们去看哪些小分子能够与FAM171A2结合,把结合力最高的前几位小分子作为候选干预分子,在体外实验和疾病模型上验证其是否能够起到阻断作用,这样就非常高效。”
郁金泰估测,得益于AI辅助科研的手段,团队在5年内就完成了原本需要几十年甚至更长时间才能完成的工作。
最终,团队在7000余种小分子中成功找到了一种小分子化合物bemcentinib,在体外和体内试验中证实其可有效抑制FAM171A2和病理性α-突触核蛋白结合。
正如郁金泰所言,团队突破传统的“假说驱动”研究范式,采取AI辅助、数据驱动的创新科研范式,找到了这一存在于“既有知识体系之外”的全新蛋白。而这次,并不是郁金泰团队第一次尝试将AI与医学结合。
3个月前,郁金泰、毛颖团队和类脑智能科学与技术研究院程炜、冯建峰团队联合发表于《细胞》杂志(Cell)的交叉研究成果,同样遵循“数据驱动”理念。他们纳入所有健康相关表型和所有疾病,刻画血浆蛋白与它们的关联,全面绘制人类蛋白质组表型组图谱,相当于给人类的生命健康领域绘制一张“地图”。这意味着不久的未来,只需采一次外周血,对血浆进行蛋白检测,就能精准预测数百种疾病的患病风险。

▲
复旦交叉研究成果登上《细胞》(Cell)2025年开年封面
目前,团队已提交基于干预FAM171A2治疗帕金森病的国际专利申请,下一步将集中力量全面、系统地开展针对抑制FAM171A2与病理性α-突触核蛋白相互作用的小分子药物、抗体疗法以及基因治疗手段的临床前研发工作,并进一步将相关成果推向临床试验和临床应用,建立全球首个能够有效阻断帕金森病进展的创新性治疗手段。
回首五年探索之路,郁金泰对“原始创新”有了更深刻的理解——生物医药领域发展到现阶段,依靠单一学科、遵循传统研究范式取得重大突破将变得困难重重,多学科交叉合作、创新研究范式则是破局之道。
论文链接:https://www.science.org/doi/10.1126/science.adp3645
粤港澳大湾区精准医学研究院
GREATER BAY AREA INSTITUTE OF PRECISION MEDICINE
 公众号二维码
公众号二维码
版权所有© 粤港澳大湾区精准医学研究院 粤ICP备2021038868号 粤公网安备 44011502000710号
